
肿瘤前沿|深圳龙岗中心医院张灵艳团队开发一种可持续ROS循环发生器,助力精准抗癌
在抗击肿瘤的漫长战役中,科学家们不断寻找能够精准打击癌细胞、同时减少对正常组织伤害的“智能武器”。化学动力学疗法(CDT)作为一种新兴策略,因其高选择性和低耐药性备受瞩目。然而,肿瘤内部复杂的“微环境”——如细胞外基质(ECM)构成的致密屏障、活性氧(ROS)生成不足等——如同坚固的“铜墙铁壁”,严重限制了CDT的疗效。
2025年12月18日,深圳市龙岗中心医院张灵艳团队与中国科学院深圳先进技术研究院刘成波团队合作,在期刊 Materials Today Bio(影响因子:10.2,JCR:Q1)上发表了题为“A Sustainable ROS Cycle Generator (SRCG) for Tumor Chemodynamic Therapy”的研究论文。
他们研究开发了一种可持续ROS循环发生器(SRCG),能够连续产生ROS以实现高效肿瘤CDT。 SRCG 采用多孔金属-有机框架材料(Cu-ZIF8)作为载体,同步递送葡萄糖氧化酶(GOX)和透明质酸酶(HAase)。该方法构建出高效纳米反应器Cu-ZIF8@GOX@HAase(CZGH),可在酸性条件下释放GOX 和HAase以水解葡萄糖和透明质酸。生成的产物可与CZ中的铜离子反应,产生高浓度 ROS,促进肿瘤细胞死亡。此外, CZGH 可降解细胞外基质(ECM)并增强肿瘤通透性,从而促进其递送并缓解缺氧。这使得葡萄糖能够渗透至肿瘤组织,确保血流中葡萄糖向 SRCG 系统的充足供应,进而实现可持续ROS生成。 SRCG 在CDT中的有效性已在体外和乳腺癌小鼠模型的体内研究中得到证实凸显了其作为突破性肿瘤治疗策略的潜力。

一、研究背景与设计思路
尽管CDT利用肿瘤微环境中过表达的H₂O₂通过类芬顿反应产生高毒性羟基自由基(·OH),具有高选择性、低耐药性等优势,但其疗效受限于TME中H₂O₂本底浓度低、肿瘤细胞抗氧化能力强以及致密ECM导致的药物渗透困难与缺氧。本研究旨在通过纳米工程策略同步解决上述问题。核心设计思路为:利用HAase降解ECM主要成分透明质酸(HA),改善肿瘤渗透性与营养输送;引入GOX催化葡萄糖氧化生成H₂O₂,实现肿瘤内H₂O₂的自供给与扩增;并借助Cu掺杂ZIF-8(CZ)的类过氧化物酶活性,高效催化H₂O₂转化为·OH,同时利用其类过氧化氢酶活性再生氧气,形成自我维持的催化循环。
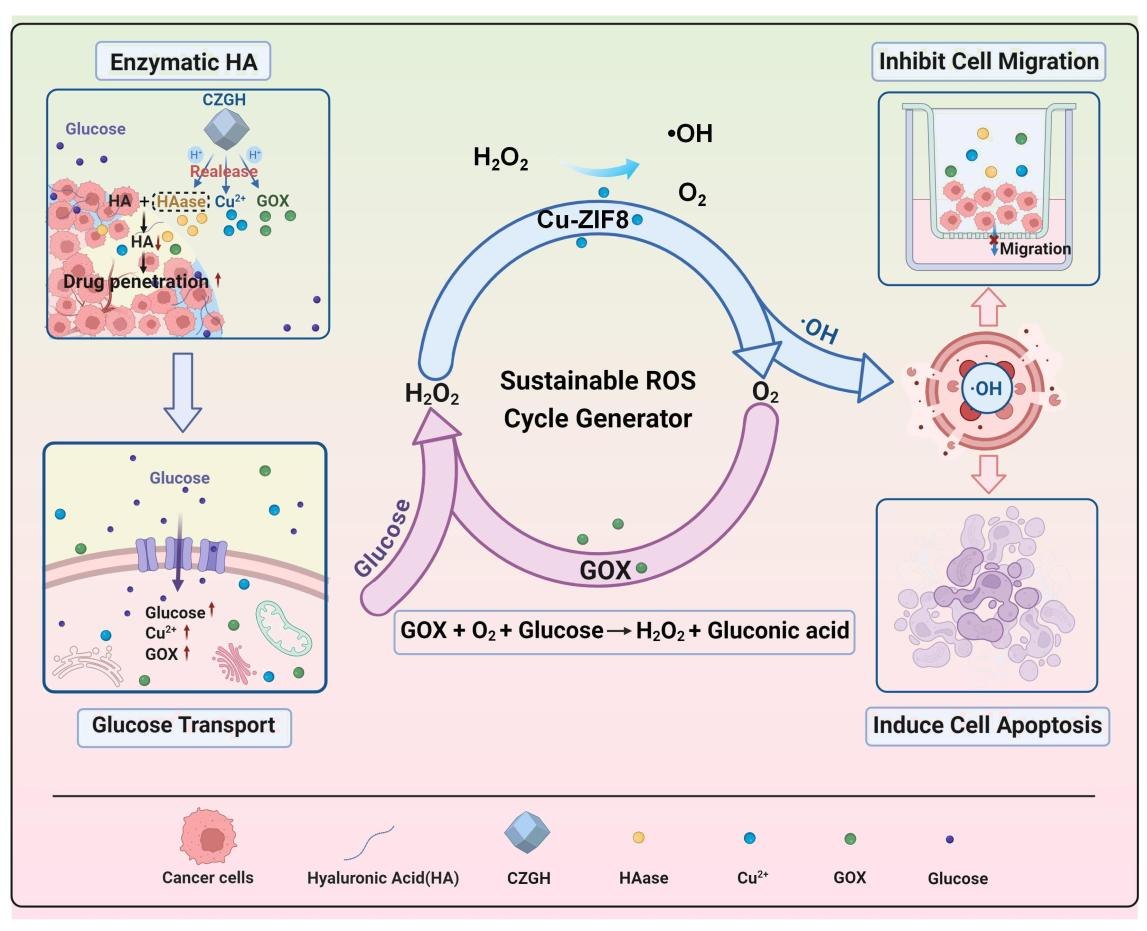
CZGH纳米平台的构建与工作机制 研究团队合成的CZGH以Cu²⁺掺杂的ZIF-8(CZ)为载体,共装载GOX与HAase。该纳米颗粒具备良好稳定性与pH响应性,能在肿瘤酸性微环境(pH 6.5)中特异性降解并释放双酶。其协同工作机制如图1所示:1)ECM重塑:释放的HAase降解HA,降低组织间压,显著增强纳米颗粒及葡萄糖等小分子的肿瘤渗透性,缓解缺氧;2)底物自供给与ROS生成:渗透性改善后,内流葡萄糖被GOX催化氧化生成H₂O₂与葡萄糖酸(酸化局部环境);3)可持续ROS循环:生成的H₂O₂在酸性环境下被CZ中Cu⁺/Cu²⁺通过类芬顿反应高效转化为·OH,攻击肿瘤细胞。同时,CZ的类过氧化氢酶活性分解部分H₂O₂产生氧气,反馈供给GOX催化反应,从而形成“GOX耗糖产H₂O₂ → Cu催化产·OH/O₂ → O₂支持GOX”的自我维持循环,实现ROS的持续产生。
二、体外及体内功能验证
材料表征与功能验证表明,CZGH在模拟ECM中能有效增强染料渗透,并展示出葡萄糖浓度依赖的H₂O₂生成、酸性增强的类过氧化物酶活性及显著的氧气再生能力,证实了其设计功能。体外抗肿瘤研究显示,CZGH能被4T1乳腺癌细胞高效内吞,并以剂量依赖性方式显著降低细胞活力,其细胞毒性主要源于级联反应产生的·OH。此外,CZGH有效抑制了癌细胞的迁移、侵袭能力,并显著降低细胞内ATP水平、提升ROS水平,证实了“饥饿-氧化”协同作用。肿瘤渗透性评估通过3D肿瘤球及荷瘤小鼠模型证实,得益于HAase的作用,CZGH相比对照组展现出更深的肿瘤穿透深度与更优的分布,并能破坏肿瘤球结构完整性。体内治疗效能在4T1乳腺癌小鼠模型中得到验证。光声成像显示CZGH治疗后肿瘤氧饱和度显著提升,证实其缓解缺氧的能力。治疗结果表明,CZGH组肿瘤生长抑制效果最为显著,且小鼠体重及主要器官未出现异常。组织学分析(H&E、Ki-67、TUNEL染色)进一步显示CZGH能有效诱导肿瘤细胞凋亡、抑制增殖。生物安全性评估证实CZGH溶血率低,对正常内皮细胞毒性小,体内未见明显系统性毒性或器官损伤,具备良好的生物相容性。
本研究成功构建了一种集ECM重塑、底物自供给与可持续ROS循环生成于一体的智能纳米反应器CZGH。其创新性在于通过多模块协同,将肿瘤微环境中的限制性因素(致密基质、缺氧、H₂O₂不足)转化为治疗优势,实现了化学动力学疗效的显著提升。该策略不仅为克服实体瘤(尤其是富含基质的肿瘤)的治疗阻力提供了新思路,其自我维持的催化循环设计理念也为开发下一代多模式协同的纳米药物奠定了基础。未来研究可聚焦于优化金属离子控释动力学、探索主动靶向策略,以进一步推动其临床转化。
【团队负责人】

论文信息:
Yuling Zhang, Silue Zeng, et al. “A Sustainable ROS Cycle Generator (SRCG) for Tumor Chemodynamic Therapy.” Materials Today Bio (2025). https://doi.org/10.1016/j.mtbio.2025.102709
来源:深圳市抗癌协会


