
翰宇药业:国产GLP-1要在美国放大招!
近期,深圳翰宇药业股份有限公司(以下简称“翰宇药业”)宣布,其自主研发的GLP-1利拉鲁肽注射液正式获得美国食品药品监督管理局(FDA)上市批准,是首个在美国获批的利拉鲁肽注射液仿制药(即“首仿药”)。
利拉鲁肽注射剂目前仍处于美国短缺药品目录内,市面上供不应求的状态。这对翰宇药业而言,利拉鲁肽在美成功获批,不仅是翰宇药业国际化发展的重要里程碑,也代表了翰宇药业的技术水平和产品质量国际领先。
十年磨一剑
翰宇药业的出海“阳谋”
翰宇药业利拉鲁肽在美国成功上市的背后,是十年磨一剑的韧劲,将出海作为第二生命曲线,就需要在质量控制、杂质研究等方面做到国际领先。
然而,翰宇药业在出海布局方面已经走在前列,始终坚持早期确立的“立足中国,放眼全球”国际化战略方针,武汉原料药生产基地、坪山制剂生产基地按照当今世界最高标准即cGMP标准设计兴建,引进国际领先的生产技术和先进设备,目前坪山制剂生产基地、武汉原料药生产基地、龙华总部研发中心等均已通过FDA cGMP标准现场检查,后两者更是“零缺陷”通过。

翰宇药业(武汉)有限公司成立于2014年,2019年正式投产。作为原料药生产基地,翰宇武汉生产车间设计超前,规模宏大,设备设施先进,合成仪、裂解仪、高效液相色谱仪等均为国外进口设备;工艺设计合理,同时具备固相、液相车间,针对不同品种,有多种工艺路线选择,达到成本、质量最优化;产线多样且共线无干扰,目前其多肽原料药年产量已达吨级以上。


2013年,深圳坪山制剂生产基地建成投产,同样引进国际先进水平的生产线,包括卡式瓶注射笔自动组装线、原装进口全自动西林瓶灌装联动线等,均配备有先进完善的质量体系。并采用了全自动化控制,由系统程序自动运行,为公司产品的质量控制提供了强有力的保障。


在产线设计上尚且如此提早布局,不难看出这是一场发展战略的“阳谋”—出海。
翰宇药业26年以来深耕多肽药物制造领域,也正是26年以来的技术经验积累,铸就了国际化发展的里程碑。FDA的审评权威性代表着医药监管领域的最高标准与严谨态度,成功拿下利拉鲁肽美国首仿,也为翰宇药业后续产品进入国际市场提供实践经验和坚实基础。
海外再造一个“翰宇”
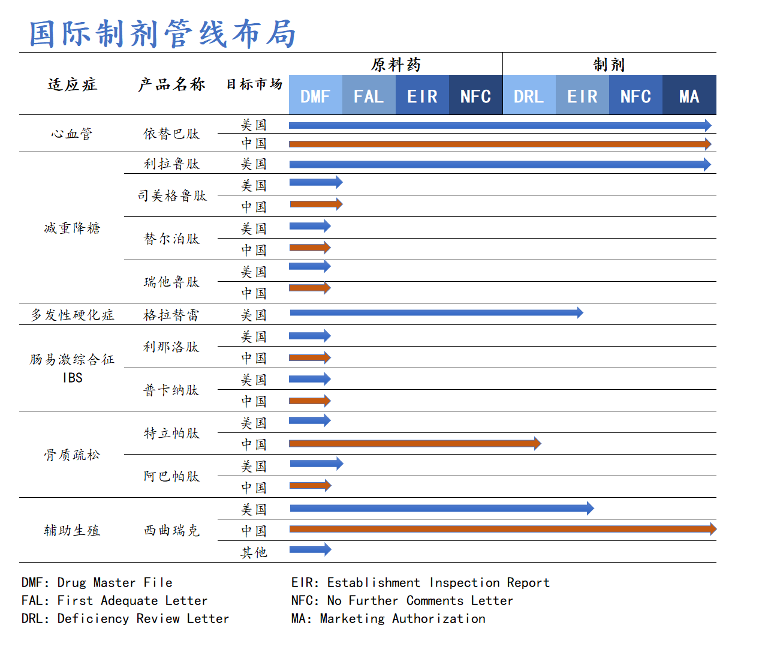
翰宇药业GLP-1管线首个重磅制剂在美国获得FDA正式批准上市,得益于翰宇药业前瞻性的管线生命周期管理布局,以及持续的研发投入,未来管线上的制剂产品还包括司美格鲁肽、替尔泊肽、瑞他鲁肽、格拉替雷等等,也将陆续进入加速阶段。
2024年前三季度,翰宇药业研发费用占营业收入的18.22%,公司已打造完成多肽药物从原料药到制剂的研发与生产全产业链开发平台,大力推动技术改进和产能提升,并且被广东省科技厅列为“广东省多肽药物工程技术研究开发中心”,被国家发改委列为“多肽药物国家地方联合工程实验室”,屡获深圳市市长奖、广东省科学技术奖、广东省制造业500强等殊荣。

目前,翰宇药业产品在海外市场已经形成批量突破,正式进入收获期,未来市场渗透潜力不容小觑,公司国际收入的财务表现也进入增长通道。
原料药端,翰宇药业能够实现几乎所有已上市多肽药物原料药的开发和生产,并对长链多肽原料药(氨基酸数量在30个以上)的开发具有独到的技术优势,尤其是在利拉鲁肽、司美格鲁肽、替尔泊肽以及格拉替雷等产业化方面,在国际上具有较高知名度,目前公司已有30多个多肽原料药取得《药品生产许可证》。
制剂端,翰宇药业的利拉鲁肽已经与跨国药企达成全球市场拓展授权合作,覆盖美国、加拿大、德国、法国等30多个国家及地区;与三生蔓迪就司美格鲁肽注射液(减重适应症)产品中国、墨西哥、巴西、中东等国家和地区展开合作;与辉凌医药就辅助生殖领域达成战略合作,合作范围覆盖全球78个国家和地区。
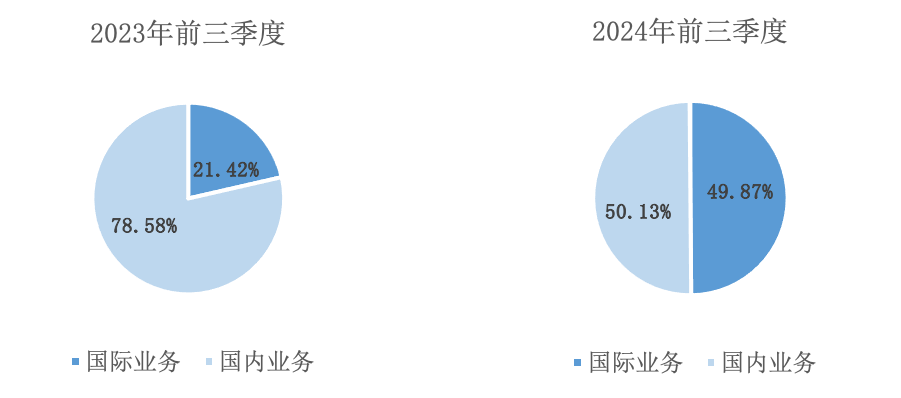
随着公司国际市场的不断突破,翰宇药业的海外营收实现了大幅度的飞跃, 2024年前三季度,公司国际出口业务同比增速高达117.53%,占总营收比重达49.87%。而在2023年前三季度,海外营收占比仅为21.42%。
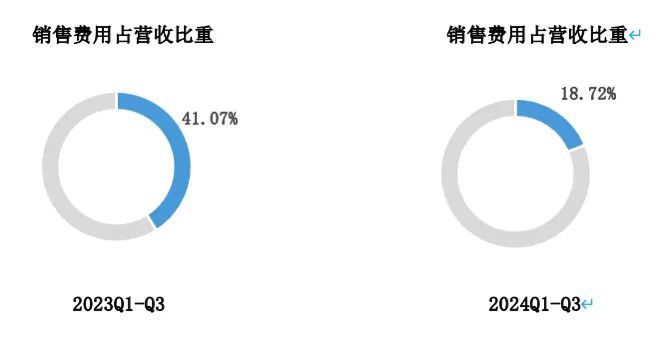
从费用端看,近几年翰宇药业销售费用呈下降趋势,2024年前三季度销售费占营业总收入比例降低至18.72%,相较于2023年前三季度41.07%的占比有明显优化。
得益于营收结构变化,以及License-out交易模式的优势,翰宇药业无论在收入增长还是成本控制方面,竞争优势将进一步扩大。
国产多肽制剂在海外崛起
潜力十足
多肽类药物以连续多年的高增长势头受到业界瞩目。2023年,全球多肽药物规模已达795亿美元,根据弗若斯特沙利文数据,中国多肽药物市场从2016年的57.5亿美元上升至2020年的81.3亿美元,年复合增速达9%,约为全球药物市场规模整体增速的2倍。
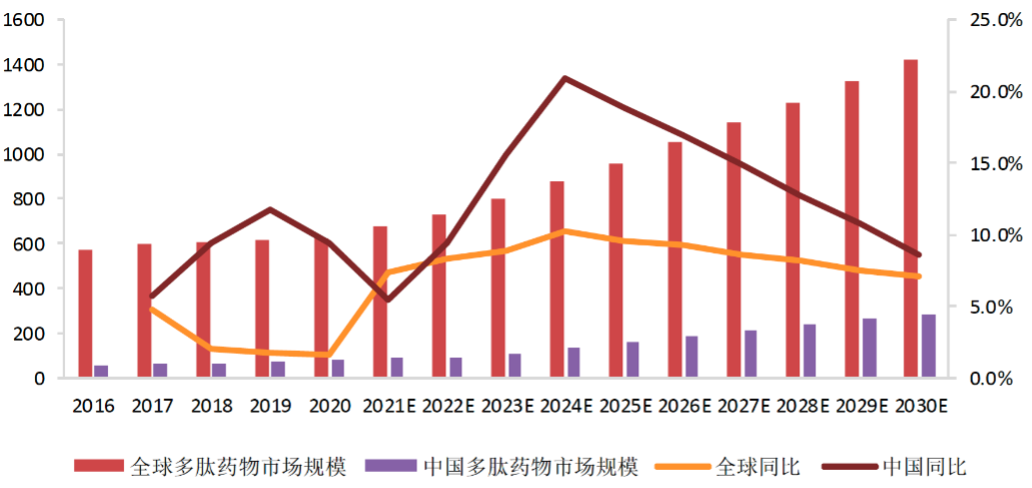
多肽药物中,以GLP-1为首的多肽药物迅速上涨,正在引领行业迈向加速发展,且当前很多海外公司积极布局引进管线,其中GLP-1减重代谢相关药物是一大热门品种。而中国,随着创新药的不断发展,将成为全球减重药物市场的重要参与者。
原研药仍短缺
首仿药上市将帮助到更多患者
截至今日,FDA短缺药目录(Shortage list)显示处于供不应求的短缺状态,我们注意到,第一次进入美国FDA短缺药品目录在2023年7月18日,后于2024年12月16日FDA再次更新状态,依然显示短缺。

另外,基于药房公开数据显示,美国终端单支笔的售价约300美金/支。这意味着,翰宇药业的利拉鲁肽注射液以首仿药身份登陆美国,将帮助到更多有需要的患者。这对翰宇药业而言,不仅是其国际化发展里程碑式的机会,也代表了翰宇药业的技术水平和产品质量国际领先。
商业模式方面与Hikma签署了美国的独家授权合作,除出货价交易金额外,后续还将根据Hikma的该产品净销售额计算后端双位数分成。
此次正式在美上市后,将成为公司业绩全新的增长点,国产GLP-1即将在美国放大招!
(免责声明:此文内容为本网站刊发或转载企业宣传资讯,仅代表作者个人观点,与本网无关。仅供读者参考,并请自行核实相关内容。)


